ในการที่จะให้นิยามของกรด- เบส และในการจำแนกสารต่างๆ ว่าเป็นกรดหรือเบสนั้นได้มีนักวิทยาศาสตร์ ได้ศึกษาและตั้งทฤษฎีกรด- เบส ขึ้นหลายทฤษฎีด้วยกัน ทฤษฎีกรด- เบสที่สำคัญมีดังนี้
ทฤษฎีกรด- เบสของอาร์เรเนียส
อาร์เรเนียส เป็นนักวิทยาศาสตร์ชาวสวีเดน ได้ตั้งทฤษฎีกรด- เบส ในปี ค. ศ. 1887 ( พ. ศ. 2430) อาร์เรเนียสศึกษาสารที่ละลายน้ำ (Aqueous solution) และการนำไฟฟ้าของสารละลายนั้น เขาพบว่าสารอิเล็กโทรไลต์จะแตกตัวเป็นไอออน เมื่อละลายอยู่ในน้ำและให้นิยามกรดไว้ว่า“ กรด คือ สารที่เมื่อละลายน้ำแล้วแตกตัวให้ไฮโดรเจนไอออน” เช่น
HCl (g)
HClO4(l)
“ เบสคือ สารที่เมื่อละลายน้ำแล้วแตกตัวให้ไฮดรอกไซด์ไอออน” เช่น
NaOH (s)
KOH (s)
ข้อจำกัดของทฤษฎีกรด - เบส อาร์เรเนียส
- ทฤษฎีกรด- เบส อาร์เรเนียส จะเน้นเฉพาะการแตกตัวในน้ำ ให้เป็น H+ และ OH- ไม่รวมถึงตัวทำละลายอื่นๆ ทำให้อธิบายความเป็นกรด- เบสได้จำกัด
- สารที่ี่จะเป็นกรดได้ต้องมี H+ อยู่ในโมเลกุล และสารที่ี่จะเป็นเบสได้ก็ต้องมี OH- อยู่ในโมเลกุล
กรด คือ สารที่ี่สามารถให้โปรตอนกับสารอื่นๆ ได้ (Proton donor)
เบส คือ สารที่ี่สามารถรับโปรตอนจากสารอื่นได้ (Proton acceptor)
พิจารณาตัวอย่างต่อไปนี้
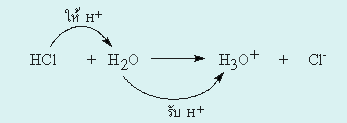
H2O เป็นสารที่ี่รับโปรตอน (H+) ดังนั้น H2Oจึงเป็นเบส
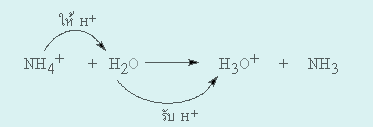
H2Oเป็นสารที่ี่รับโปรตอน (H+) ดังนั้น H2Oจึงเป็นเบส
ข้อจำกัดของทฤษฎีกรด - เบสของเบรินสเตต- ลาวรี
ทฤษฎีกรด- เบสของเบรินสเตต- ลาวรี ใช้อธิบายสมบัติของกรด- เบส ได้กว้างกว่าทฤษฎีของอาร์เรเนียส แต่ยังมีข้อจำกัดคือ สารที่จะทำหน้าที่เป็นกรดจะต้องมีโปรตอนอยู่ในสารนั้นสารที่เป็นได้ทั้งกรดและเบส
(Amphoteric)สารบางตัวทำหน้าที่เป็นทั้งกรด เมื่อทำปฏิกิริยากับสารตัวหนึ่ง และทำหน้าที่เป็นเบส เมื่อทำปฏิกิริยากับอีกสารหนึ่ง นั่นคือเป็นได้ทั้งกรดและเบส สารที่มีลักษณะนี้เรียกว่า สารเอมโพเทอริก(Amphoteric) เช่น H2O , HCO3- เป็นต้น
กรณีของ H2O

ดังนั้นอาจจะสรุปได้ว่า สารที่เป็นเอมโฟเทอริก ถ้าทำปฏิกิริยากับสารที่ให้โปรตอนได้ดีกว่า ตัวมันเองจะรับโปรตอน ( ทำหน้าที่เป็นเบส) แต่ถ้าไปทำปฏิกิริยากับสารที่ให้โปรตอนได้ไม่ดี ตัวมันเองจะเป็นตัวให้โปรตอนกับสารนั้น ( ทำหน้าเป็นกรด)
ทฤษฎีกรด- เบสของลิวอีส
ในปี ค. ศ. 1923 ( พ. ศ. 2466) ลิวอีสไดเสนอนิยามของกรดและเบสดังนี้กรด คือ สารที่สามารถรับอิเล็กตรอนคู่ จากเบส แล้วเกิดพันธะโคเวเลนต์
เบส คือ สารที่สามารถให้อิเล็กตรอนคู่ในการเกิดพันธะโคเวเลนต์
ปฏิกิริยาระหว่างกรด- เบส ตามทฤษฎีนี้ อธิบายในเทอมที่มีการใช้อิเล็กตรอนคู่ร่วมกัน กรดรับอิเล็กตรอนเรียกว่าเป็น Electrophile และเบสให้อิเล็กตรอนเรียกว่าเป็น Nucleophile และตามทฤษฎีนี้สารที่เป็นเบสต้องมีอิเล็กตรอนคู่อิสระ เช่น

ทฤษฎีของลิวอิสนี้มีข้อดีคือ สามารถจำแนกกรด- เบส ที่ไม่มีทั้ง H หรือ OH- ในสารนั้น และแม้ว่าสารนั้นไม่ได้อยู่ในรูปสารละลาย แต่อยู่ในสถานะแก๊สก็สามารถใช้ทฤษฎีลิวอิสอธิบายความเป็นกรดเบสได้
ไม่มีความคิดเห็น:
แสดงความคิดเห็น