ความแรงของกรดและเบส
การเปรียบเทียบความแรงของกรดและเบส อาจจะพิจารณาได้ดังนี้
1. ดูจากการแตกตัวของกรด
กรดที่มีการแตกตัวมาก มีความเป็นกรดมาก กรดและเบสที่แตกตัวได้ 100% จะเรียกว่ากรดแก่ และเบสแก่ ตามลำดับ ซึ่งสามารถนำไฟฟ้าได้ดี แต่ถ้ากรดและเบสนั้นแตกตัวได้เพียงบางส่วนก็จะเรียกว่า กรดอ่อน หรือเบสอ่อน ตามลำดับ ซึ่งการนำไฟฟ้าจะไม่ดี
สำหรับการพิจารณาค่าการแตกตัวของกรดและเบสนั้น นอกจากจะคิดจากเปอร์เซ็นต์การแตกตัว หรืออาจจะดูได้จากค่าคงที่สมดุลของการแตกตัวของกรดหรือเบส (Ka หรือ Kb) เช่น
ความแรงของเบส พิจารณาจากค่า Kb กล่าวคือ ถ้ามีค่า Kb มาก มีความเป็นเบสมากกว่า Kb น้อย เช่น
NH3 Kb = 1.76 x 10-5
N2H4 Kb = 9.5 x 10-7
ความเป็นเบส NH3> N2H4
2. ดูจากความสามารถในการให้และรับโปรตอน
กรดแก่ ได้แก่ กรดที่ให้โปรตอนได้มาก
กรดอ่อน ได้แก่ กรดที่ให้โปรตอนได้น้อย
เบสแก่ ได้แก่ เบสที่รับโปรตอนได้มาก
เบสอ่อน ได้แก่ เบสที่รับโปรตอนได้น้อย
โดยมีข้อสังเกตเกี่ยวกับคู่กรด- เบส ดังนี้
- ถ้ากรดเป็นกรดแก่ คู่เบสจะเป็นเบสอ่อน เช่น
HCl (aq) + H2O  H3O+ (aq) + Cl- (aq)
H3O+ (aq) + Cl- (aq)
กรดแก่ เบสอ่อน
- ถ้ากรดเป็นกรดอ่อน คู่เบสจะเป็นเบสแก่ เช่น
HS- (aq) + H2O 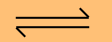 H3O+ + S2- (aq)
H3O+ + S2- (aq)
กรดอ่อน เบสแก่
- ถ้าเบสเป็นเบสแก่ คู่กรดจะเป็น กรดอ่อน เช่น
H3O+ + S2-(aq) 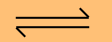 HS- (aq) + H2O
HS- (aq) + H2O
เบสแก่ กรดอ่อน
- ถ้าเบสเป็นเบสอ่อน คู่กรดจะเป็น กรดแก่ เช่น
Cl-(aq) + H3O+ 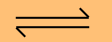 HCl + H2O
HCl + H2O
เบสอ่อน กรดแก่
3. ดูจากการเรียงลำดับในตารางธาตุ
การพิจารณาความแรงของกรดและเบสดูจากการเรียงลำดับของธาตุที่อยู่ในกรดนั้้้น ตามตารางธาตุ ซึ่งแบ่งออกได้เป็น
3.1 กรดออกซี หมายถึง กรดที่ประกอบด้วย H, O และธาตุอื่นอีก เช่น HNO3 ,H3PO4,H3AsO4 ,HClO4 ถ้าจำนวนอะตอมออกซิเจนเท่ากัน ความแรงของกรดเรียงลำดับดังนี้
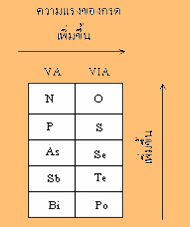
ดังนั้น H2SO4 > H2SeO4 , H3PO4 > H3AsO4
3.2 กรดที่ไม่มีออกซิเจน เช่น HCl, HBr, HF, และ HI ความแรงของกรดแรงลำดับดังนี้
HI > HBr > HCl > HF
H2S > H2O
ไม่มีความคิดเห็น:
แสดงความคิดเห็น